�����ĺ�Ĭ����һ��Ӱ��㷺���������Լ��������־�ԵIJ��������Ǧ�-���������ij�������ԭ��ά�IJ��ᡣ��ȥ�������ѧ������Ϊ��-���������׳����밢���ĺ�Ĭ���ķ����йأ�Ҳ����˲��ٰ����-����������ҩ�Ȼ�����������Ժ��ٿ�����ȫ�����ŷ�����Ч��

���գ������ڡ���Ȼ���ӿ�Nature Communications�ϵ�һ���о��������ǽ�����һ����Ȥ�ķ��֣���ʵ�����������о��Ħ�-���������ף��ڽṹ���뻼�ߴ�����Ħ�-�������������ź����ԵIJ�ͬ��������ܹ����ͣ�Ϊ��ʵ�����е�һЩ�鵤��ҩ���ڻ�������ȴ��ʧЧ��
�����о��ɵ¹��ڶ�ķ��ѧ��Ulm University���Ŀ�ѧ�������������о�����Ǵ����������ĺ�Ĭ����������Ĵ�����֯�﴿�����˦�-����������ԭ��ά����ʹ���䶳�羵����������нṹ����������������������������ߵĦ�-����������ԭ��ά��̬��Ȼ������ͬ�����ڽṹ���кܸߵ�����ԡ�
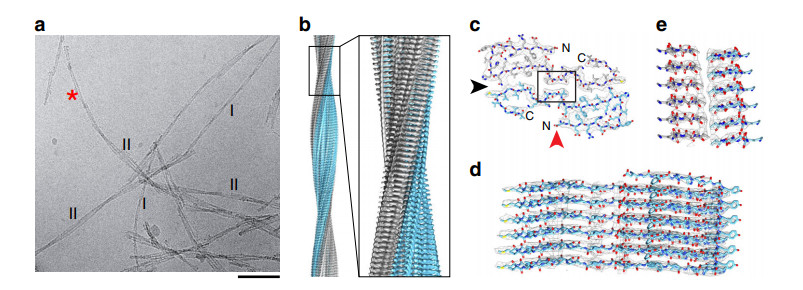
���䶳�羵�����۲쵽�Ľṹ��ͼƬ��Դ���ο�����[1]��
����˼���ǣ���ͨ����ѧ�ϳɻ��������������Ħ�-����������ԭ��ά��ȣ����ߴ�������²����ṹ���������Ľṹ���졣Ʃ�磬�����ȡ�������������������ṹ��left-hand twisted�����������еĵ��ף����������ṹ��right-hand twisted�������⣬����ǰ�ķ��������ȣ����ǵ����۵���ʽҲ�����ԵIJ�ͬ��
�����ĵ����ۻ��ڣ������DZ�ʾ���������ֵ������ṹ���dz���Ȥ������ǿ�����о���ʵ���ߴ�����������Ҫ�ԡ�������������Ҳ�����ر�ʾ����Ȼ�۲쵽�˲�ͬ��������������ϳɵĦ�-����������ԭ��ά��һ���뼲���ء����DZ��ص�ָ������Щ���ֱ�������������ϳɦ�-����������ԭ��ά��ʹ�õ����������������ڵ���ʵ�����Щ��ͬ�������˽ṹ�ϵIJ��졣��Щ����ľ���Ӱ�죬����Ҫ��һ����̽����
����Ȼ���ṩ�����ż��ָ���������о������������Ⱒ���ĺ�Ĭ�����µ�ͻ��Ԧµ���������Ӱ�죬�������ڿ�����ֹ����ԭ��ά�γɵ�ҩ���
�ο����ϣ�[1] Kollmer, M., Close, W., Funk, L. et al. Cryo-EM structure and polymorphism of A�� amyloid fibrils purified from Alzheimer��s brain tissue. Nat Commun 10, 4760 (2019) doi:10.1038/s41467-019-12683-8



 ��ҵ�����Ĵ���������
��ҵ�����Ĵ���������